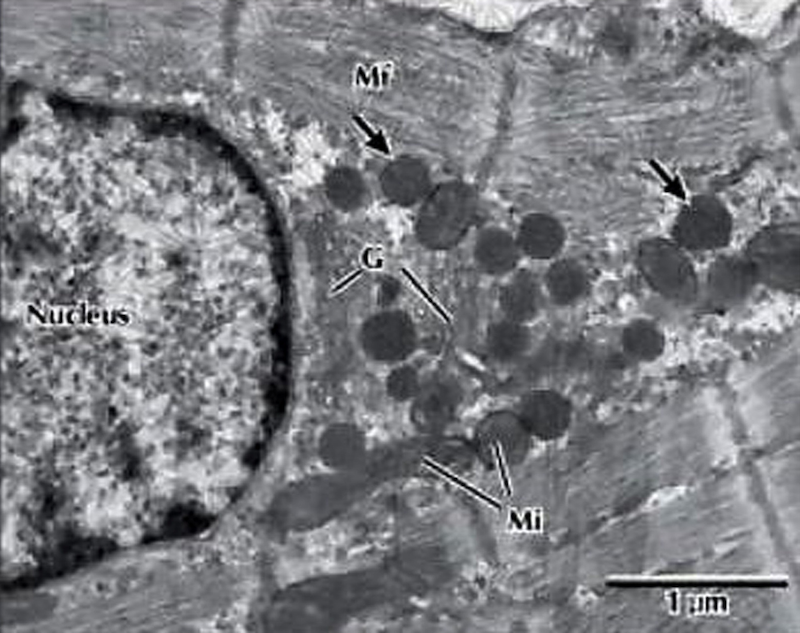
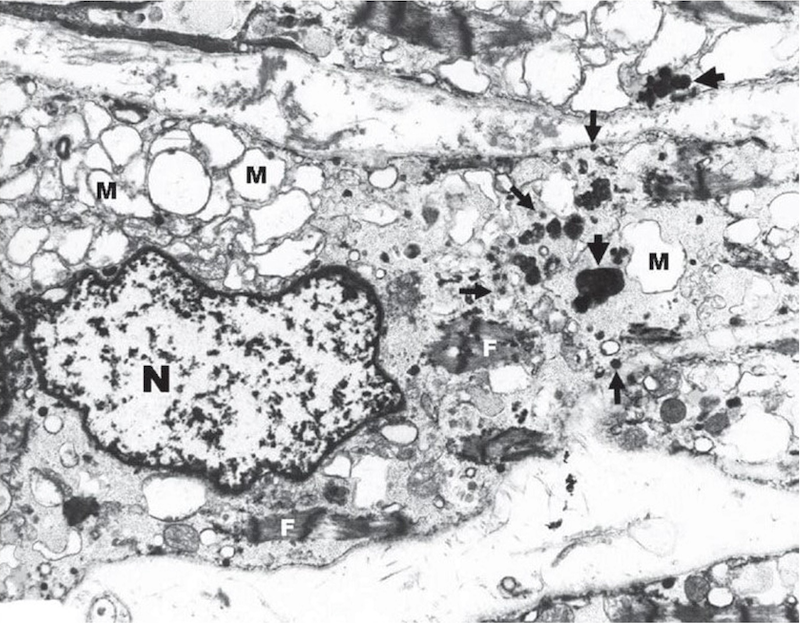
Effets des ERO sur un cardiomyocyte, état préclinique.
Le fer lié à la Tf se lie au TfR-1, est endocytosé et entre dans le pool de fer labile cytoplasmique où il est stocké
dans la ferritine ou utilisé dans les processus cellulaires. En cas de surcharge de fer, la Tf est saturée et le FNLT
est détectable. Le FNLT pénètre dans la cellule de manière non régulée par le biais du DMT-1, du Zip 14 et du LVDCC. Des
ERO sont générés, lesquels peuvent endommager les protéines, les lipides et les acides nucléiques; les protéines
endommagées comprennent notamment les myofibrilles, qui affectent la contractilité, et les caspases, qui contrôlent la
mort cellulaire; les dommages lipidiques peuvent conduire à la lyse des cellules et des organites, et à l'altération de
la fluidité membranaire et de la fonction des canaux; les dommages à l'ADNmt peuvent réduire la production d'énergie.
Les effets subcellulaires des ERO provenant de l'excès de fer sur les cardiomyocytes peuvent expliquer l'incidence
accrue des événements cardiaques cliniques dans les cas de SMD.
1
Les données précliniques indiquent une réduction des concentrations cardiaques de fer non hémique chez les souris traitées par des inhibiteurs des canaux calciques de type L2
ADN, acide désoxyribonucléique; ADNmt, ADN mitochondrial; DMT-1, transporteur des métaux divalents 1; ERO, espèces réactives de l'oxygène; FNLT, fer non lié à la transferrine; LVDCC, canal calcique de type L dépendant du rythme cardiaque; RTf, récepteur de la transferrine; Zip-14, transporteur du zinc.
1. Kim CH & Leitch HA. Crit Rev Oncol Hematol. 2021;163, avec permission; 2. Liu Q et al. Assemblée annuelle 2021 de l'American Society of Hematology. Résumé 758.